5月13日,国家药监局发布2025年度药品审评报告,药品制剂注册申请总量、创新药获批数量等均创历史新高,其中2025年批准创新药76个,包括新机制新靶点药物11个。从治疗领域来看,抗肿瘤仍是获批创新药集中领域,2025年全年共有34款抗肿瘤药物获批,占比达44.74%。
获批创新药数量创新高
按照我国药品注册分类相关标准,2025年共批准上市1类创新药76个品种,数量再创新高。2024年我国批准上市的1类创新药为48个品种。在2025年获批的创新药中,26个品种(34.2%)通过优先审评审批程序批准上市;15个品种(19.7%)附条件批准上市;15个品种(19.7%)在临床试验期间纳入了突破性治疗药物程序。
1类创新药实现的往往是“从无到有”的突破,即针对长期缺乏有效治疗手段的疾病,其研发门槛也相对较高。新京报记者统计了76个创新药的治疗领域,同往年情况类似,抗肿瘤药仍是获批创新药的集中领域,2025年共有34个创新药为抗肿瘤药物,占比为44.74%,也是唯一一个获批创新药数量达到两位数的治疗领域。抗感染药物(8个)、内分泌系统疾病药物(7个)、皮肤及五官科药物(5个)紧随其后。
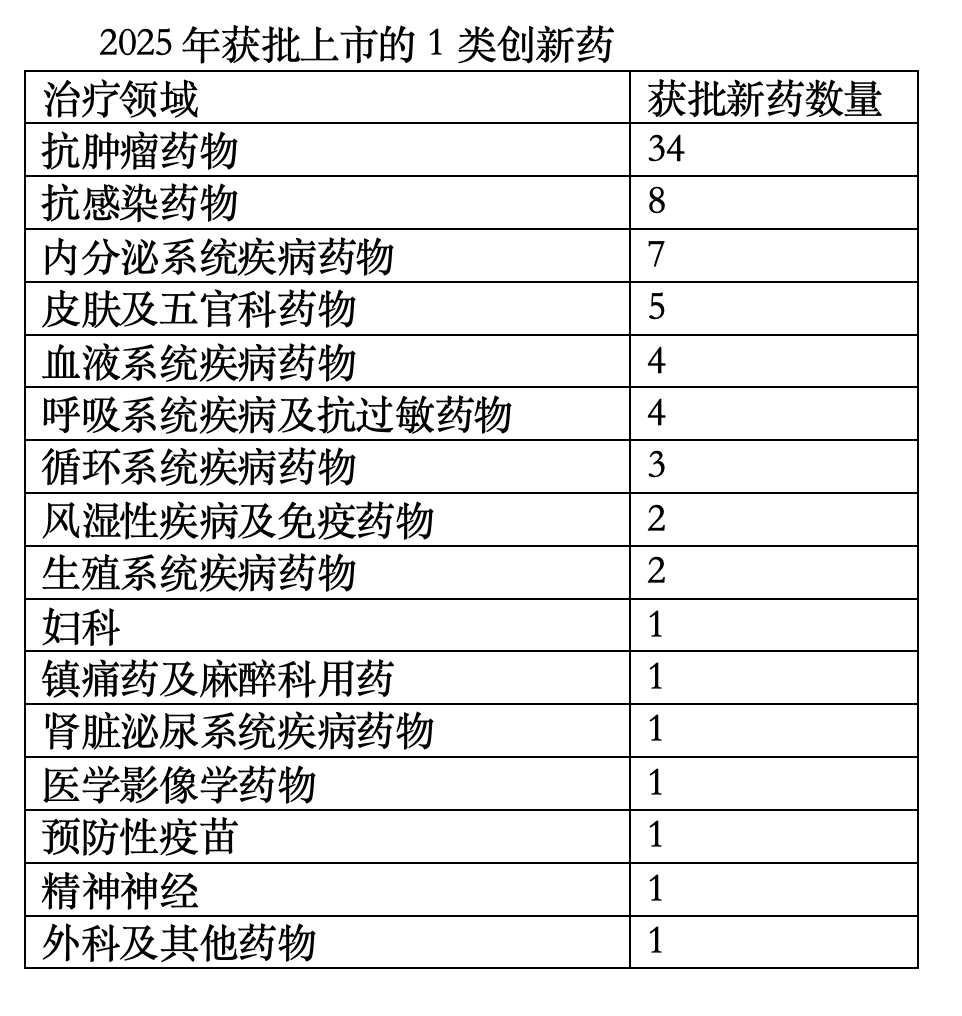
新京报记者根据2025年度药品审评报告统计。
从药物类型来看,76个1类创新药中共有47个化学药品、23个生物制品(1个预防用生物制品、22个治疗用生物制品)以及6个中药。
一同创新高的还包括药品注册申请申报量等多个数据。2025年,药审中心受理各类注册申请20149件,同比增加3.00%,这也是近五年(2021-2025年)的最高水平,其中药品制剂注册申请、化学原料药注册申请数量也均为近五年最高水平。以注册申请类别统计,2025年共受理临床试验申请3756件,新药上市许可申请(NDA)663件,亦为今年最高水平。
多个“指标”增加的背后,是新药审评审批过程的提速。突破性治疗药物程序是新药审评审批“提速”途径之一。2025年国家药监局共收到突破性治疗药物程序申请424件,同意纳入突破性治疗药物程序101件,占申请数量的23.82%,较2024年增加10.99%。此外,具有明显临床价值的药品,可以申请优先审评审批。适用优先审评审批程序的上市注册申请的审评时限也由常规程序的200日缩短为130日,其中临床急需境外已上市罕见病用药的审评时限为70日。2025年共纳入优先审评审批注册申请133件(92个品种),同比增加7.26%。
“提速”还在继续。2025年9月12日,国家药监局发布《关于优化创新药临床试验审评审批有关事项的公告》,对获得国家全链条支持创新药发展政策体系支持的具有明显临床价值的重点创新药品种、审评中心公布的符合条件的儿童创新药、罕见病创新药,以及中药创新药品种、全球同步研发品种的临床试验申请,在受理后30个工作日内完成审评审批,进一步支持以临床价值为导向的创新药研发,提高临床研发质效。
6个品种放射性药品获批
从药物种类来看,罕见病、儿童用药等重点领域也有不少新药获批。国家药监局2025年全年批准罕见病用药48个品种,其中12个品种(24.5%)通过优先审评审批程序加快上市;全年批准儿童用药138个品种,其中25个品种(18.1%)通过优先审评审批程序加快上市,另批准40个品种扩展儿童适应症。
2025年还有6个品种的放射性药品获批,其中3个品种(50.0%)通过优先审评审批程序加快上市。作为近年来备受关注的新赛道,越来越多的放射性药品获批。放射性药物是指含有放射性核素,供医学诊断和治疗用的一类特殊药物,主要包括诊断放射性药物和治疗性放射性药物两大类,近年来由诊断用产品开始用于治疗层面,由于能够精准识别并杀死癌细胞,放射性疗法被形象地称为具备精准打击肿瘤细胞能力的“肿瘤定位导弹”。有数据显示,2023年到2029年,全球核药市场将从126亿美元增长到210亿美元,复合年增长率约为8.3%。在国内核药市场,中国放射性药物市场规模在2030年有望增长至260亿元,包括远大医药、复星医药、中国同辐等在内的多家企业也在布局。
监管也在同步跟进。2025年,国家药监局完善放射性药物的审评标准体系,制定《放射性治疗药物申报上市临床风险管理计划技术指导原则》,以进一步为放射性药物临床研发提供指导和服务。
新京报记者 张秀兰
校对 赵琳












